| Tematický plán Po jednorázovém připomenutí základů první pomoci (Elektro č. 11) si nyní stanovíme „tematický plán„ okruhů, kterým se budeme v dalších číslech Elektra v rubrice Repetitorium věnovat. Vzhledem k rozsahu tematického plánu předpokládáme jeho naplnění v letech 2007 až 2008. 1. Fyzika, matematika, elektrotechnika
1.1. Skladba hmoty
1.2. Základní pojmy, veličiny a jednotky
1.3. Základní zapojení obvodů a součástek 2. Schémata, značky, dokumentace
2.1. Technické kreslení a dokumentace
2.2. Schémata, značky a označování 3. Měřicí technika
3.1. Elektrická měření
3.2. Měření neelektrických veličin 4. Elektrické instalace
4.1. Instalace nízkého napětí
4.2. Inteligentní instalace 5. Elektrická zařízení
5.1. Výroba a rozvod elektrické energie
5.2. Elektrické stroje
5.3. Elektrické spotřebiče 6. Elektronika
6.1. Polovodičové materiály a prvky
6.2. Výkonová elektronika 7. Elektrotechnické vybavení budov
7.1. Základy automatizační techniky
7.2. Informační, komunikační a automatické systémy 1. Skladba hmoty Při uvádění látky na téma Skladba hmoty nemíníme řešit žádné hlubší otázky elementární fyziky. Budeme vycházet ze zjednodušené představy všeobecně podávané v současných učebních textech. 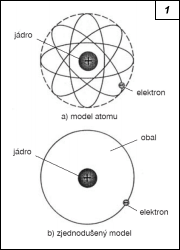 Obr. 1. Bohrův model atomu vodíku Struktura a stavba hmoty byly vědecky zkoumány ve snaze vysvětlit podstatu elektrických (elektrostatických) jevů. Koncem 19. století a na počátku 20. století se na základě dosavadních vědeckých poznatků dospělo k názoru, že všechny látky (hmota) se skládají z atomů (atomos – řecky „nedělitelný„). Atom je částice o tak malé velikosti, že jej nelze pozorovat ani pod mikroskopem. Jeho průměr je přibližně 1/10000 µm = 10–10 m = 0,1 nm. Energetické vlastnosti atomů však mají zásadní význam pro vlastnosti hmoty. Bylo zjištěno a dokázáno, že atom se skládá z dalších energetických částic; odtud také interpretace, že vlastně jde o „chomáče energie„, resp. částice na pomezí hmoty a energie. Po původním planetárním Rutherfordově modelu atomu (Skot lord Ernest Rutherford, 30. 8. 1871 až 19. 10. 1937) byl v roce 1913 vytvořen známý Bohrův model atomu (obr. 1, dánský fyzik Niels Henrik David Bohr, 7. 10. 1885 až 18. 11. 1962). Ten byl v roce 1925 doplněn o Pauliho princip na vlnově mechanický model atomu (švýcarský fyzik rakouského původu Wolfgang Pauli, 25. 4. 1900 až 15. 12. 1958) Atom se skládá z jádra a obalu. Průměr jádra je přibližně 100 000krát menší než průměr obalu. Atom je tvořen elementárními částicemi: jádro se skládá z nukleonů, tj. protonů a neutronů, obal tvoří elektrony (obr. 2, příklad stavby atomu lithia). Neutrony jsou elektricky neutrální částice a neovlivňují elektrické vlastnosti látek. Protony (v jádru, s kladným nábojem) a elektrony (na obalu, se záporným nábojem) mají opačné elektrické náboje (stejné velikosti) a vzájemně se přitahují. 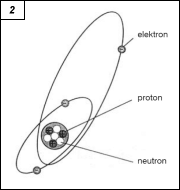 Obr. 2. Stavba atomu lithia Protony a elektrony se nazývají nosiče nábojů. Nesou nejmenší možný elektrický náboj, tzv. elementární náboj e = 1,602 × 10–19 C (coulombů*)). Hmotnost elektronů je 1 836krát menší než hmotnost nukleonů. Ty mají navzájem téměř stejnou hmotnost. Pohyb elektronů není nahodilý, ale musí odpovídat přesně danému systému vycházejícímu z energetických poměrů látky. Elektrony se proto pohybují po zcela určitých drahách, na kterých mají zcela určitou energii – jsou na konkrétní energetické hladině. Obal atomu se dělí na vrstvy (resp. slupky), kterých je maximálně sedm a tyto vrstvy se dále dělí na hladiny. Pro příklad uvádíme atom prvku lithium (obr. 2). Je to kov s nejjednodušší stavbou atomu – ve vnitřní vrstvě má dva elektrony, ve vnější jeden. Jeho jádro se skládá ze tří protonů a čtyř neutronů. Atom se chová neutrálně – záporný náboj tří elektronů ve vrstvách je vyvážen kladným nábojem tří protonů v jádru. Je-li atom ve stavu, kdy se počet elektronů liší od počtu protonů, není elektricky neutrální a nazývá se iont (řecky ion – pohybující se). Ionty vznikají z neutrálních atomů odnětím nebo přijetím elektronu do vrstvy. Odebráním elektronů převáží kladný náboj (kladný iont). Při zvýšení počtu elektronů převáží záporný náboj (záporný iont). (jk; pokračování)
*) Charles Augustin de Coulomb, francouzský fyzik, 17. 6. 1736 až 23. 8. 1806 | 




